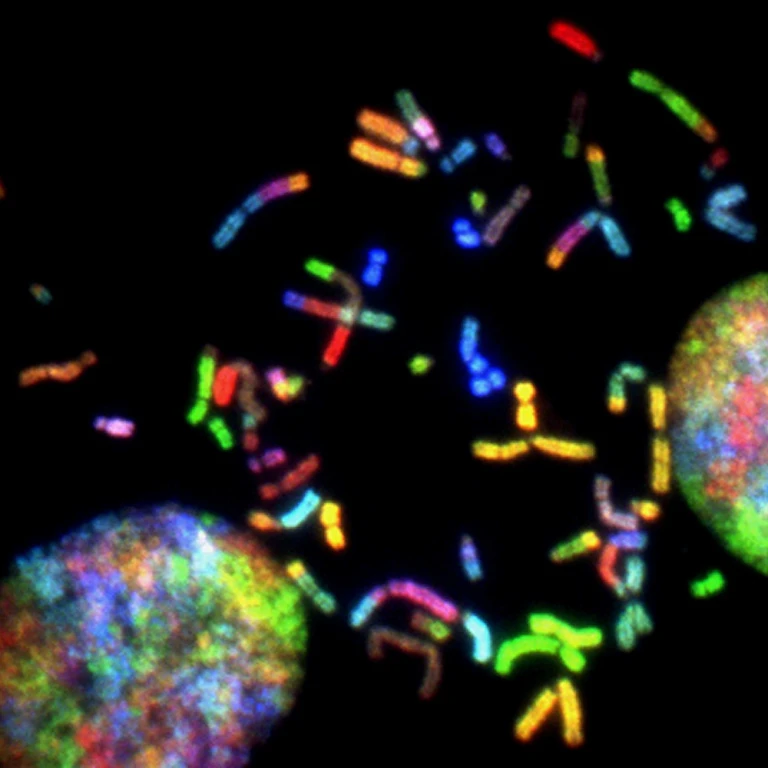Rôle central de l’hybridation in situ dans la biologie moléculaire
L’hybridation in situ est une technique de biologie moléculaire qui permet de localiser précisément des séquences d’ADN ou d’ARN dans des cellules intactes. Cette technique d’hybridation repose sur l’appariement complémentaire entre une sonde marquée et une séquence cible présente dans des coupes de tissus ou dans des cellules en suspension. En biotechnologie, l’hybridation in situ relie directement la structure moléculaire à l’organisation histologique du tissu.
Dans sa forme la plus classique, l’hybridation in situ utilise des sondes d’ADN ou d’ARN simple brin, souvent appelées sonde mono brin, qui reconnaissent des acides nucléiques spécifiques. Ces sondes peuvent être marquées par de la biotine ou de la digoxygénine, ce qui permet ensuite une détection enzymatique via des enzymes de phosphatase alcaline ou d’autres systèmes. L’objectif est de visualiser l’expression des gènes dans leur contexte cellulaire, sans extraire l’ADN ARN de l’échantillon.
Les techniques d’hybridation in situ se déclinent en plusieurs variantes, dont la situ hybridization en fluorescence, souvent appelée fluorescence FISH, et la situ HIS en coloration enzymatique. La microscopie de fluorescence permet alors d’observer la localisation des signaux dans les noyaux ou le cytoplasme, tandis que la microscopie optique classique révèle des tailles de grains colorés autour des séquences cibles. Pour l’analyste du secteur biotech, ces approches d’analyse moléculaire sont devenues des standards de technique de laboratoire.
De l’ADN à l’ARN messager : ce que révèle l’hybridation in situ
L’hybridation in situ offre une passerelle unique entre génomique et histologie, car elle permet de suivre l’ADN, l’ARN et l’ARN messager dans les mêmes coupes de tissus. En ciblant une séquence cible d’ADN ARN par une sonde spécifique, la technique révèle si un gène est présent, amplifié ou réarrangé dans un noyau donné. En parallèle, l’hybridation in situ appliquée à l’ARN messager renseigne sur l’expression des gènes dans des types cellulaires précis.
Les techniques d’hybridation dérivées des approches Southern Northern ont structuré ce champ, en combinant la rigueur de l’analyse moléculaire avec la finesse de la microscopie. La situ hybridation de type FISH, qui utilise des sondes fluorescentes, permet par exemple de suivre plusieurs gènes en parallèle grâce à des couleurs distinctes. Cette microscopie de fluorescence, appliquée à des coupes tissus, révèle des signaux ponctuels dont les tailles de grains reflètent parfois le niveau d’expression.
Pour les entreprises de biotechnologie engagées dans les essais cliniques, l’hybridation in situ devient un outil de stratification des patients. Comprendre l’expression gènes dans des tumeurs ou des tissus inflammatoires aide à sélectionner les volontaires pour un essai clinique rémunéré en France. Ainsi, la technique de laboratoire qu’est la situ hybridization s’intègre directement dans la chaîne de décision clinique et réglementaire.
Hybridation in situ, FISH et enzymes de phosphatase : principes de détection
Deux grandes familles de techniques d’hybridation in situ dominent aujourd’hui la pratique en biotechnologie, avec d’un côté la FISH fluorescente et de l’autre les méthodes enzymatiques à la phosphatase alcaline. La fluorescence FISH repose sur des sondes marquées par des fluorochromes, détectées ensuite par microscopie de fluorescence à haute résolution. Les signaux lumineux, souvent ponctuels, indiquent la présence de séquences cibles d’ADN ARN ou d’ARN messager dans les noyaux ou le cytoplasme.
Les méthodes enzymatiques utilisent au contraire des sondes couplées à la biotine ou à la digoxygénine, révélées par des anticorps associés à des enzymes de phosphatase. La phosphatase alcaline transforme un substrat incolore en un précipité coloré, générant des tailles de grains visibles en microscopie optique classique. Cette approche reste très utilisée pour l’analyse histologique tissu, notamment dans les laboratoires où la microscopie de fluorescence est moins accessible.
Pour les acteurs industriels, le choix entre FISH et techniques enzymatiques dépend du coût, de la sensibilité et de la compatibilité avec les flux de travail numériques. Les plateformes de pathologie numérique, dont le modèle économique rappelle celui d’une application de gestion de santé, privilégient souvent la fluorescence FISH pour sa quantification plus aisée. Cependant, les techniques d’hybridation enzymatiques restent incontournables pour certaines analyses de routine en hybridation situ et en situ HIS.
Applications en embryologie, oncologie et diagnostic moléculaire
En embryologie, l’hybridation in situ permet de suivre l’expression des gènes dans les embryons à différents stades de développement. Les sondes d’ARN mono brin ciblant l’ARN messager révèlent comment des gènes de développement s’activent dans des régions précises des tissus embryonnaires. Cette analyse spatiale de l’expression gènes éclaire les mécanismes qui relient séquence cible et morphogenèse.
En oncologie, la situ hybridization de type FISH est devenue un standard pour détecter des amplifications de gènes, des translocations chromosomiques ou des pertes de segments d’ADN. Les coupes tissus tumorales sont alors examinées en microscopie de fluorescence, et les tailles de grains lumineux indiquent le nombre de copies de gènes dans chaque cellule. Ces techniques d’hybridation situ orientent le choix de thérapies ciblées, en complément d’analyses de type Southern Northern réalisées sur ADN ARN extrait.
Dans le diagnostic moléculaire de routine, les laboratoires combinent souvent hybridation in situ, immunohistochimie par anticorps et autres tests de biologie moléculaire. Les enzymes de phosphatase et la phosphatase alcaline restent des outils robustes pour révéler des sondes marquées à la biotine digoxygénine dans des tissus fixés. Pour les ingénieurs biomédicaux, ces approches s’inscrivent dans un continuum d’innovations détaillé dans l’analyse du génie médical appliqué à la santé, où la situ hybridization occupe une place stratégique.
De la coupe histologique au signal : étapes clés en laboratoire
La réussite d’une hybridation in situ commence par la préparation rigoureuse des coupes de tissus ou des cellules. Les coupes tissus doivent conserver l’intégrité de l’ADN, de l’ARN et de l’ARN messager, tout en permettant la pénétration des sondes mono brin. Le choix du fixateur, de l’épaisseur de coupe et des conditions de déparaffinage influence directement la qualité des signaux observés en microscopie.
Vient ensuite l’étape d’hybridation situ proprement dite, où la sonde spécifique est appliquée sur la séquence cible dans le tissu. Les paramètres de température, de salinité et de durée d’incubation conditionnent la spécificité de l’appariement entre acides nucléiques complémentaires. Une hybridation trop permissive génère des signaux non spécifiques, tandis qu’une hybridation trop stricte peut masquer une faible expression gènes.
Après les lavages, la détection fait intervenir soit la fluorescence FISH, soit des systèmes enzymatiques à base d’enzymes de phosphatase. La phosphatase alcaline, couplée à des anticorps dirigés contre la biotine digoxygénine, produit des tailles de grains colorés dans les zones où la sonde s’est fixée. Les analystes interprètent ensuite ces signaux à l’aide de la microscopie de fluorescence ou de la microscopie optique, en les reliant aux structures observées dans l’histologique tissu.
Enjeux industriels, automatisation et perspectives pour l’hybridation in situ
Pour l’industrie biotech, l’hybridation in situ et la situ hybridization en fluorescence représentent des marchés en forte structuration. Les fabricants développent des automates capables de gérer l’ensemble du flux, depuis la préparation des coupes tissus jusqu’à l’analyse d’images en microscopie de fluorescence. Cette automatisation vise à standardiser les techniques d’hybridation et à réduire la variabilité entre laboratoires.
Les plateformes d’analyse numérique exploitent des algorithmes pour quantifier l’expression des gènes à partir des signaux FISH ou enzymatiques. En combinant les données issues de l’hybridation situ, des approches Southern Northern et d’autres tests moléculaires, elles construisent des profils complets d’ADN ARN et d’ARN messager. Ces profils soutiennent des décisions cliniques plus fines, notamment dans la sélection de thérapies ciblées et la conception de nouveaux essais cliniques.
Dans ce contexte, la maîtrise de la situ HIS, de la fluorescence FISH, des enzymes de phosphatase et des systèmes biotine digoxygénine devient un enjeu de compétitivité. Les entreprises qui intègrent ces techniques de laboratoire à leurs pipelines de R&D renforcent leur crédibilité scientifique et réglementaire. Pour les personnes en quête d’informations, comprendre les principes de l’hybridation in situ aide à mieux appréhender la valeur réelle des diagnostics moléculaires proposés sur le marché.
Données chiffrées clés sur l’hybridation in situ
- Part estimée des tests d’hybridation in situ dans le diagnostic moléculaire hospitalier, en pourcentage du volume total d’analyses.
- Proportion de laboratoires de pathologie utilisant la fluorescence FISH pour l’oncologie, comparée aux méthodes enzymatiques à la phosphatase alcaline.
- Temps moyen nécessaire pour réaliser une hybridation in situ complète, depuis la préparation des coupes tissus jusqu’à la lecture en microscopie.
- Nombre moyen de gènes analysés simultanément par FISH multiplexe dans les plateformes de biologie moléculaire.
- Taux de croissance annuel du marché mondial des réactifs et automates dédiés à l’hybridation in situ.
Questions fréquentes sur l’hybridation in situ
À quoi sert l’hybridation in situ en pratique clinique et en recherche ?
L’hybridation in situ sert à localiser des séquences d’ADN ou d’ARN directement dans les cellules et les tissus, ce qui permet de relier l’expression des gènes à des structures histologiques précises. En pratique clinique, elle est utilisée pour le diagnostic de cancers, d’anomalies chromosomiques et de certaines maladies infectieuses. En recherche, elle éclaire les mécanismes de développement, de différenciation cellulaire et de réponse aux traitements.
Quelle différence entre FISH et les méthodes enzymatiques à la phosphatase alcaline ?
La FISH utilise des sondes fluorescentes détectées par microscopie de fluorescence, ce qui permet souvent une analyse multiplexe et une quantification plus fine. Les méthodes enzymatiques reposent sur des sondes marquées à la biotine ou à la digoxygénine, révélées par des enzymes de phosphatase alcaline produisant un précipité coloré visible en microscopie optique. Le choix dépend des équipements disponibles, du type d’échantillon et des objectifs de sensibilité ou de débit.
Pourquoi parle-t-on de techniques Southern Northern en lien avec l’hybridation in situ ?
Les termes Southern et Northern renvoient à des méthodes historiques d’hybridation sur membranes, respectivement pour l’ADN et l’ARN. Ces approches ont posé les bases conceptuelles de l’hybridation, en montrant comment des sondes mono brin peuvent reconnaître des séquences cibles spécifiques. L’hybridation in situ transpose ces principes directement dans les tissus, en conservant l’architecture cellulaire.
Quels types d’échantillons peuvent être analysés par hybridation in situ ?
Les principaux échantillons sont les coupes de tissus fixés et inclus en paraffine, les coupes congelées et les préparations cellulaires en suspension. L’hybridation in situ s’applique aussi bien à des tissus tumoraux qu’à des embryons, des biopsies d’organes ou des cultures cellulaires. Le protocole doit cependant être adapté à la nature du tissu et à la stabilité de l’ARN messager ciblé.
Quelles compétences sont nécessaires pour mettre en place l’hybridation in situ en laboratoire ?
La mise en place de l’hybridation in situ requiert une maîtrise des techniques de laboratoire en histologie, en biologie moléculaire et en microscopie. Les équipes doivent savoir optimiser les conditions d’hybridation, de lavage et de révélation, tout en contrôlant la qualité des sondes et des enzymes de phosphatase. Une formation spécifique à l’interprétation des signaux, qu’ils soient en fluorescence FISH ou en coloration enzymatique, est également indispensable.